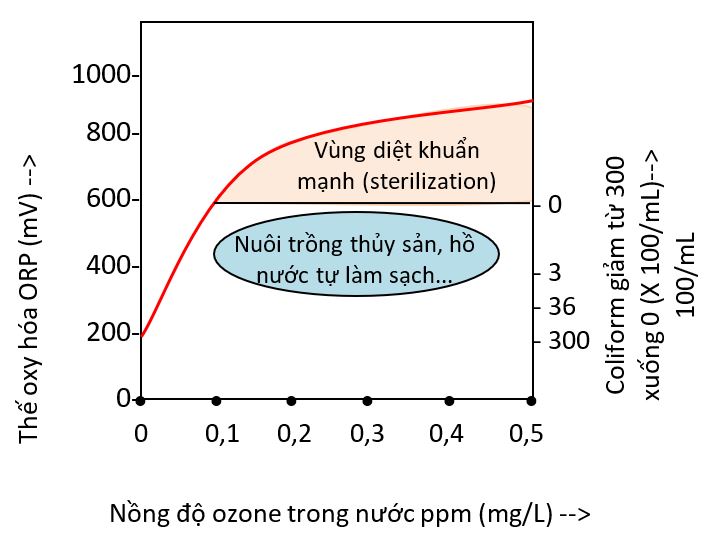
Cơ Chế Diệt Khuẩn Của Ozone (Phần 1)
Bản chất quá trình diệt khuẩn là sự tương tác giữa ozone và protein trong tế bào vi khuẩn. Ozone và các sản phẩm phân hủy của nó như oxy nguyên tử (O1), các gốc tự do phá hủy thành tế bào (chất béo phosphat) và các protein trong tế bào, làm mất cấu trúc và chức năng của tế bào.
1. Thành Phần Chính Của Cơ Thể Sống Là Protein
Vi sinh vật thường là đơn bào với cấu trúc gồm: thành tế bào, bào quan, bào tương, nhân và DNA, RNA. Các thành phần này đều là hợp chất hữu cơ phức tạp gồm ba nhóm chính: protein, carbohydrate và chất béo.
Ozone tương tác với các hợp chất này theo cơ chế oxy hóa và ozone hóa, phá vỡ các liên kết như C=C thành C=O, từ đó làm biến tính và mất chức năng sinh học của protein.
Protein là thành phần thiết yếu của sự sống. Trong tế bào, tất cả các bào quan đều chứa protein. Virus cũng cấu tạo từ vỏ protein là chủ yếu. Protein chiếm khoảng 20% cơ thể con người, chỉ sau nước (65%).
Cấu Tạo Cơ Bản Của Protein
Protein được tạo thành từ các acid amin (20 loại) kết nối với nhau bằng liên kết peptid. Mỗi acid amin gồm nhóm carboxyl (COOH), nhóm amin (NH2) và nhóm chức R.
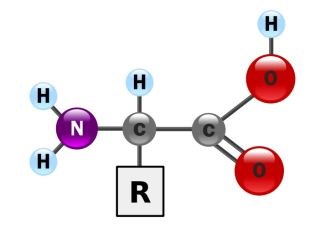
Hình 8.1: Phân tử acid amin - mắt xích cơ bản của protein.
Liên Kết Peptid Và Cấu Trúc Protein
Các acid amin nối với nhau bằng liên kết peptid tạo ra chuỗi protein.
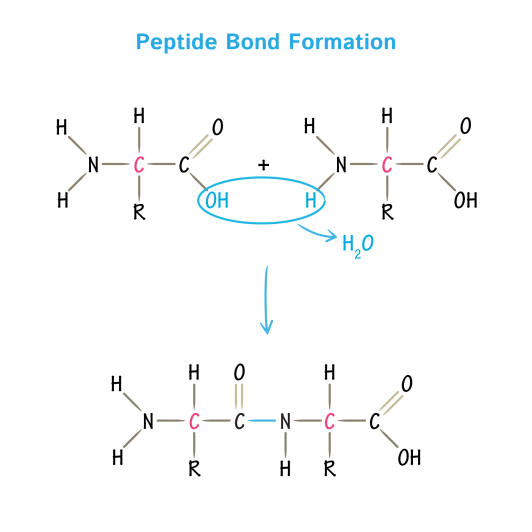
Hình 8.2: Liên kết peptid tạo ra chuỗi protein.
Cấu trúc protein gồm 4 cấp độ:
- Sơ cấp: Chuỗi acid amin.
- Thứ cấp: Cấu trúc xoắn, gấp khúc.
- Ba chiều: Cấu trúc không gian 3D.
- Bậc bốn: Nhiều chuỗi protein liên kết.
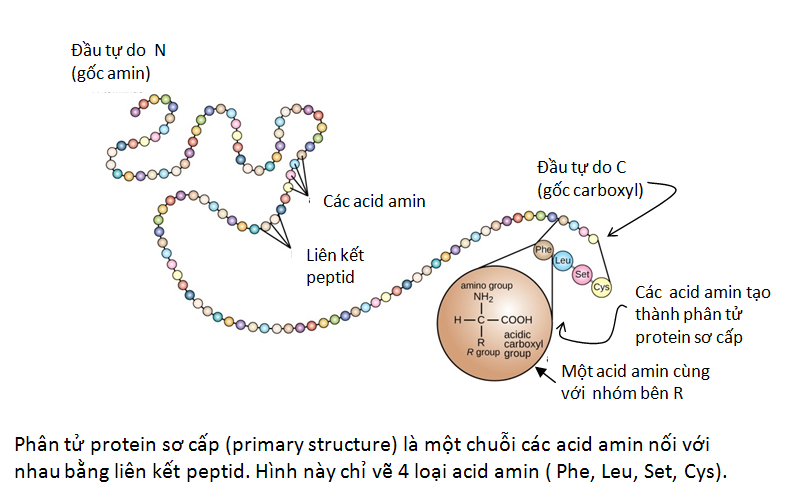
Hình 8.3: Chuỗi acid amin - protein sơ cấp.
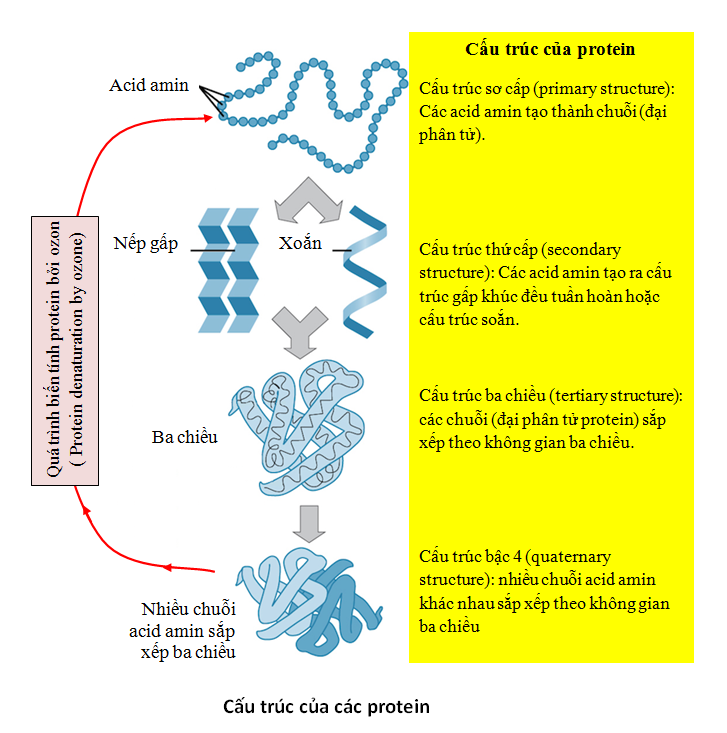
Hình 8.4: Cấu trúc không gian của protein.
Cơ Chế Oxy Hóa Của Ozone
Ozone phá vỡ các cấu trúc không gian của protein thông qua quá trình oxy hóa và denaturation (biến tính), làm mất các chức năng sinh học quan trọng như:
- Xúc tác enzyme.
- Vận chuyển chất dinh dưỡng.
- Cấu tạo các bộ phận cơ thể.
- Điều phối hoạt động của các cơ quan.
- Bảo vệ cơ thể (kháng thể).
- Truyền thông tin trong tế bào.
Ozone tấn công trực tiếp các liên kết C=C, phá vỡ cấu trúc protein bậc ba và bậc bốn, làm cho vi khuẩn mất khả năng sống và nhân đôi.
Liên Kết Tham Khảo
- Cơ Chế Diệt Khuẩn Của Ozone (Phần 2)
- Tìm hiểu thêm về Ozone
- Các sản phẩm liên quan đến diệt khuẩn bằng Ozone