Để khử khuẩn, nấm mốc và vi sinh vật nói chung trong nước, người ta thường trộn các chất oxy hóa như ozone, clo hay thuốc tím... vào nước. Khi chúng được hòa tan, trong nước xuất hiện thế oxy hóa - khử ORP, đơn vị đo là vôn. Đại lượng ORP là thước đo khả năng oxy hóa, khả năng diệt khuẩn của nước (tức là độ sạch khuẩn của nước) nhờ sự có mặt của các chất oxy hóa.

1. Chất oxy hóa và thế oxy hóa khử ORP
Phần lớn các chất diệt khuẩn, nấm, mốc... hoạt động theo cơ chế oxy hóa: Oxy làm cho sắt gỉ, biến thanh sắt vừa dẻo vừa cứng thành các vẩy gỉ, giòn, dễ vỡ vụn. Oxy diệt khuẩn cũng vậy, oxy phá hủy cấu trúc tế bào khuẩn và vi sinh vật nói chung, làm bất hoạt hoặc tiêu diệt chúng. Oxy (O2) chỉ là chất đại diện cho các chất oxy hóa, nhiều chất khác cũng có khả năng như oxy và còn mạnh hơn oxy như clo, ozone, hydro peroxit H2O2, thuốc tím (Na,K)MnO4 và rất nhiều chất tương tự khác. Tất cả các chất đó gọi chung là chất oxy hóa. Khả năng oxy hóa của các chất oxy hóa được đánh giá bằng thế oxy hóa khử, nói gọn là thế oxy hóa (ORP: Oxidation-Reduction Potential hay Oxidation Potential). Đại lượng này là điện thế, đo bằng vôn (V) hay milivôn (mV). Hình 1.1(A) cho thấy độ mạnh oxy hóa của các chất oxy hóa so với clo (coi độ mạnh của Cl=1).
Bảng 1.1(A). Thế oxy hóa (V) và độ mạnh oxy hóa của các chất (so với clo)
|
Tên |
Thế oxy hóa (V) |
Độ mạnh oxy hóa |
|
Flor F2 |
2,87 |
2,1 |
|
Gốc tự do OH* |
2,8 |
2 |
|
Bio-hydrox MxOyClz |
2,8-2,9 |
2 |
|
Gốc tự do sulfat SO4* |
2,5 |
1,8 |
|
Oxy nguyên tử O1 |
2,42 |
1,8 |
|
Ozone O3 |
2,05 |
1,5 |
|
Sodium persulfat Na2S2O8 |
2,0 |
1,5 |
|
Hydro peroxit H2O2 |
1,8 |
1,3 |
|
Thuốc tím Na(K)MnO4 |
1,7 |
1,2 |
|
Acid hypoclorous HOCl |
1,49 |
1,1 |
|
Clo Cl2 |
1,36 |
1 |
|
Oxy phân tử O2 |
1,2 |
0,9 |
|
Clo dioxit ClO2 |
0,95 |
0,7 |
|
Ion hypoclorid OCl2- |
0,94 |
0,7 |
|
Sodium hypoclorit NaOCl |
0,94 |
0,7 |
|
Ghi chú: Bio-hydrox MxOyClz , M: kim loại |
||
Bảng 1.1(A) cho thấy thế oxy hóa và độ mạnh oxy hóa (so với clo - chất oxy hóa thông dụng nhất) của các chất oxy hóa. Khả năng oxy hóa của ozone mạnh hơn clo 1,5 lần, gốc tự do OH* mạnh hơn 2 lần. Flo có thế oxy hóa cao nhất, tuy nhiên giá thành rất cao (~190 USD/100 g). Các gốc tự do (radical) cũng có thế oxy hóa cao, song chúng rất không bền và chỉ xuất hiện nhờ các phản ứng của clo hay ozone trong nước.
Các chất oxy hóa thường được sử dụng để diệt khuẩn, nấm, mốc trong môi trường khí và đặc biệt là trong môi trường nước. Khi cho các chất oxy hóa hòa tan vào nước, chúng phản ứng với nước vào tạo ra các ion, gốc tự do... cũng có tính oxy hóa. Nước chứa các chất oxy hóa cũng có thế oxy hóa ORP đo bằng vôn (V) hay milivôn (mV) và có khả năng diệt khuẩn.
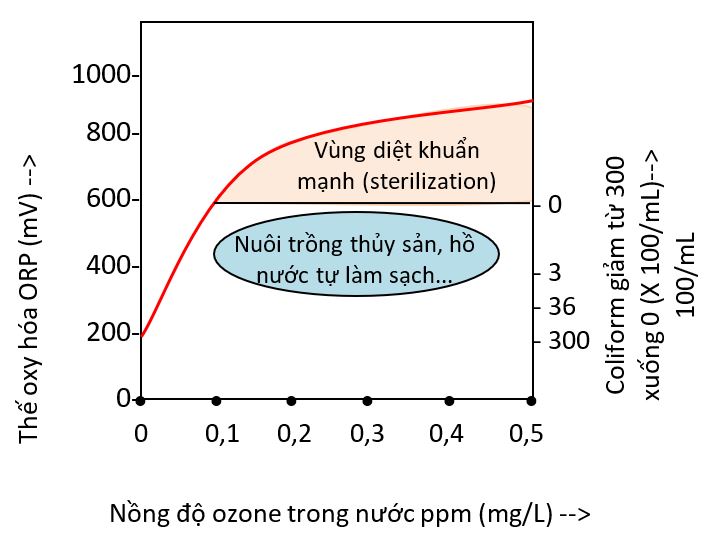
Thế ORP của nước hoặc của dung dịch cho biết khả năng khử khuẩn, nấm, mốc, vi sinh vật nói chung của nước khi các chất oxy hóa được hòa tan trong nước. Nước có ORP ³ 800 mV có khả năng diệt khuẩn rất tốt. Nước có ORP ~600 mV có khả năng dừng hoạt tính của khuẩn (hình 1.2A). Đồ thị hình 1.2A còn cho biết sự phụ thuộc của ORP vào nồng độ ozone tan trong nước. Nồng độ ozone 0,4-0,5 ppm làm cho nước có ORP ~800 mV, đủ để diệt hoàn toàn khuẩn trong nước (đơn vị đo nồng độ: ppm =1 mgO3/L, một phần triệu).
2. Độ lớn của thế oxy hóa ORP của nước nói lên rằng nước có nhiều hay ít oxy hoặc các tác nhân oxy hóa khác như ozone, thuốc tím, clo... Điều đó cũng có nghĩa là ORP chỉ ra khả năng diệt khuẩn, nấm, mốc... của nước mạnh hay yếu, và hệ quả là mức độ sạch khuẩn của nước. ORP càng cao, khả năng diệt khuẩn của nước càng mạnh, nước càng sạch khuẩn. Trong tự nhiên, các hồ nước sạch có thể có ORP tới 400-500 mV, hồ như thế có khả năng tự làm sạch. Thế oxy hóa ORP và các ứng dụng được nêu trong bảng 1.2(A). Tất cả các ứng dụng đó dựa trên khả năng kìm hãm sự phát triển, bất hoạt và tiêu diệt khuẩn của nước có ORP cao.
3. Vì sao ORP lại được đo bằng mV?
Khi một điện cực kim loại đặt trong nước hoặc một dung dịch nào đó, giữa điện cực và nước xuất hiện thế điện cực E (mV) do có sự trao đổi điện tích. Khi so sánh thế điện cực này với một điện cực chuẩn (có thế điện cực được coi bằng không hoặc cố định), nhận được thế oxy hóa khử ORP, đây là điện thế nên đo bằng mV. Nước càng nhiều oxy, ozone... thế ORP càng cao (dương). Máy đo ORP gồm hai điện cực, trong đó có một điện cực chuẩn (có thế điện cực bằng không). Một milivôn kế để đo điện thế giữa hai điện cực đó (khi hai điện cực đặt trong dung dịch) và đó chính là thế oxy hóa ORP của dung dịch.

Hình 1.2(A). Ozone tan trong nước làm tăng thế oxy hóa ORP của nước lên tới 800-900 mV. ORP khoảng ~600 mV làm vô hoạt các loại khuẩn (disinfection), ~800 mV: diệt khuẩn mạnh (sterilization). Vùng ORP thấp phù hợp trong nuôi trồng thủy sản và các ứng dụng khác.
Nguồn: Khunwang Royal Project Product Center of Mae Hia Royal Project Thailand Institute of Scientific and Technological Research (TISTR) Eastern Thai Consulting 1992 Company Limited.
4. Thế ORP liên quan đến khái niệm oxy hóa và khử
Đây là hai quá trình xảy ra đồng thời trong một phản ứng hóa học giữa hai chất. Chất mất điện tử tức là cho điện tử (donor) gọi là chất khử (reducer) cũng chính là chất bị oxy hóa (oxidised). Chất nhận điện tử (acceptor) gọi là chất oxy hóa (oxidizer) cũng chính là chất bị khử (reduced). Oxy, ozone... là chất oxy hóa (nhận điện tử) các kim loại và vi khuẩn là chất khử (cho điện tử). Nước có nhiều chất oxy hóa gọi là nước oxy hóa có thế ORP cao (dương). Trao đổi điện tử giữa oxy, ozone và vi khuẩn làm cho vi khuẩn bị chết tương tự như trao đổi điện tử giữa thanh sắt với oxy hay ozone làm cho sắt gỉ.
Bảng 1.2(A). Thế oxy hóa và phạm vi ứng dụng
|
ORP (mV) |
Ứng dụng |
|
0-150 |
Không có ứng dụng |
|
150-250 |
Nuôi trồng thủy sản |
|
250-350 |
Tháp làm mát (ngăn sự phát triển của rêu làm tắc ống nước) |
|
300-400 |
Nước hồ tự nhiên có khả năng tự làm sạch |
|
400-470 |
Bể bơi |
|
450-600 |
Spa, hot tubs (bồn tắm, sục nước nóng) |
|
600 |
Diệt, bất hoạt khuẩn (disinfection) |
|
800 |
Diệt hoàn toàn khuẩn (sterilization) |
5. Nước có ít oxy, nhiều hydro... có tính khử (cho điện tử) và gọi là nước khử. Người ta quan niệm nước khử (đôi khi gọi là nước hydrogen) là nước chống oxy hóa, tốt cho da và tế bào nói chung, nhưng nước khử không diệt được khuẩn. Nước oxy hóa diệt khuẩn tốt, song khi nồng độ chất oxy hóa quá cao thì có hại cho da và tế bào. Ví dụ nước máy sặc mùi clo là không tốt, làm xạm da. Hình 1.3A cho thấy thế oxy hóa ORP của một số đồ uống quen thuộc. Như vậy hàng ngày chúng ta sử dụng cả hai loại nước có ORP âm (tính khử) và dương (tính oxy hóa).
6. Các tác nhân oxy hóa trong nước ozone hóa. Ozone tan trong nước phản ứng với ion hydroxit OH- của nước, tạo ra các gốc tự do *OH (hydroxyl radical, hợp chất chứa điện tử đơn lẻ, không tạo cặp, ký hiệu là *):

(Chấm tròn nhỏ chỉ điện tử, gạch ngang là 2 điện tử ở hai đầu). Ozone không bền, tự phân hủy và sinh ra oxy nguyên tử: O3-->O2 + O1. Như vậy khi ozone hòa tan trong nước, luôn tồn tại đồng thời ozone O3, gốc tự do *OH và oxy nguyên tử O1. Tất cả chúng đều là các tác nhân oxy hóa mạnh, nhất là *OH và O1. (xem bảng 1.1(A)). Các tác nhân oxy hóa đó làm cho nước ozone có thế oxy hóa ORP cao, ORP ³ 800 mV. Nước chứa ozone nồng độ 0,4-0,5 ppm với ORP >800 mV có khả năng diệt khuẩn, cả vi khuẩn gram âm và gram dương, bào tử, kén và virus. Ozone loại bỏ dư lượng các chất bảo về thực vật, các chất hữu cơ tự nhiên NOM (Nutural Organic Matters) và carbon hữu cơ DOC (Dissolved Organic Carbon) tan và lơ lửng trong nước. Ngoài ra ozone còn oxy hóa và làm kết tủa ion Fe+ và Mn+, làm cho nước trong. Ozone khử mùi của nước ngầm. Vì các lý do đó mà ngày nay ozone đang dần thay thế các hợp chất clo trong các nhà máy nước qui mô hàng trăm nghìn mét khối nước ngày đêm.

Hình 1.3(A). Thế oxy hóa của các loại đồ uống quen thuộc, mV






Bình luận (1)
Phuc Hoang Trả lời
16/07/2022Bài viết rất hay và rõ ràng, thank tác giả rất nhiều