Khử Ozone Dư Bằng Chất Xúc Tác - Giải Pháp An Toàn Và Hiệu Quả
Khử ozone dư bằng chất xúc tác là phương pháp tối ưu để loại bỏ lượng ozone còn lại trong không khí và nước sau quá trình xử lý, đảm bảo an toàn cho môi trường và con người.
Chất Xúc Tác Là Gì?
Trong phản ứng hóa học, chất xúc tác là chất có khả năng làm tăng tốc độ phản ứng mà không bị tiêu hao trong quá trình phản ứng. Chất xúc tác đóng vai trò quan trọng trong xử lý nước thải bằng ozone và loại bỏ ozone dư trong không khí.
Nguyên Lý Phân Hủy Ozone Dư Bằng Xúc Tác
Phản ứng phân hủy ozone có thể mô tả như sau:
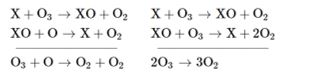
Khi có mặt chất xúc tác (ký hiệu là X), phản ứng sẽ xảy ra với tốc độ nhanh hơn và năng lượng kích thích cần thiết thấp hơn.
Cơ Chế Phân Hủy Ozone
- Ozone tiếp xúc với chất xúc tác, tạo điều kiện cho phản ứng O3 → O2 xảy ra nhanh chóng.
- Chất xúc tác tham gia vào phản ứng trung gian nhưng không bị tiêu hao.
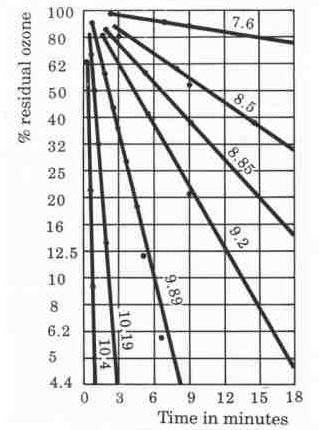
- Năng lượng kích hoạt phản ứng giảm đáng kể khi có chất xúc tác: E1 < E.
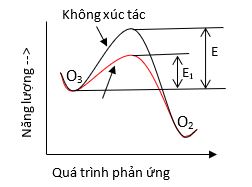
Mặc dù ozone chứa năng lượng cao hơn oxy, nhưng cần năng lượng kích hoạt ban đầu để phân hủy ozone thành oxy.
Các Chất Xúc Tác Thường Dùng Để Khử Ozone
Các chất xúc tác giúp phân hủy ozone dư có thể tồn tại dưới nhiều dạng, bao gồm:
- Các ion OH-, NO, Cl- trong không khí.
- Kim loại và oxit kim loại: Cu, Cu2O, Ag, CuO, Ag2O, Ni, Ni2O3, Fe, Fe2O3, Au, Au2O3, Pt.
- Xúc tác bề mặt: MnO2, Pt/γ-Al2O3 (Dash‐220).
Hiệu Quả Của Các Chất Xúc Tác
Theo nghiên cứu của C.Y. Chang và các cộng sự, xúc tác Pt/γ-Al2O3 (Dash‐220) có khả năng khử ozone lên đến ~99% ở nhiệt độ khoảng 60°C. Xúc tác MnO2 và hỗn hợp CuO/MnO2 cũng được chứng minh có hiệu quả cao trong việc phân hủy ozone.
Ứng Dụng Thực Tế Trong Xử Lý Ozone Dư
Các hệ thống máy ozone công nghiệp thường được tích hợp bộ khử ozone dư bằng chất xúc tác để đảm bảo an toàn. Việc khử ozone dư không chỉ giúp bảo vệ sức khỏe người sử dụng mà còn đảm bảo tiêu chuẩn môi trường.
Ngoài ra, các phụ kiện ozone như bộ lọc xúc tác, thiết bị khử ozone dư, quạt hút ozone cũng được sử dụng rộng rãi để tối ưu hóa quá trình xử lý khí thải chứa ozone.
Lợi Ích Khi Sử Dụng Xúc Tác Khử Ozone
- Tăng tốc độ phân hủy ozone dư nhanh chóng.
- Tiết kiệm năng lượng do giảm yêu cầu nhiệt độ phản ứng.
- An toàn và thân thiện với môi trường.
- Hiệu quả khử ozone lên đến 99%.
Kết Luận
Khử ozone dư bằng chất xúc tác là giải pháp an toàn, hiệu quả và được ứng dụng phổ biến trong các hệ thống xử lý ozone công nghiệp. Việc lựa chọn đúng chất xúc tác và thiết bị phù hợp sẽ giúp tăng hiệu quả xử lý và đảm bảo tiêu chuẩn môi trường.
Để được tư vấn chi tiết về thiết bị khử ozone dư và các hệ thống ozone chuyên nghiệp, vui lòng liên hệ với chúng tôi.
Liên Hệ Tư Vấn
Hotline: 0918534363 - 0912534363
Email: O3bkidt@gmail.com
Website: thietbibkidt.vn - ozonebkidt.vn